近日,深圳大学医学部生物医学工程学院董海峰教授团队与麦克马斯特大学Yingfu Li教授合作,在国际知名学术期刊Journal of the American Chemical Society(影响因子:14.5,中科院JCR一区,TOP期刊)上发表了题为“CRISPR/RNA Aptamer System Activated by an AND Logic Gate for Biomarker-Driven Theranostics”的研究论文。医学部博士后杨琦琦为第一作者,董海峰教授和Yingfu Li教授为通讯作者,深圳大学为第一完成单位。

精确诊断和治疗已成为疾病管理的关键焦点,通过根据患者独特的生物学特征定制干预措施,使治疗效果最大化,同时使副作用最小化,这种精确诊断和治疗的潜在策略包括创造能够动态适应各种病理状态的新型生物标志物应答疗法。这一策略的成功实施需要能够感知特定生物标志物并执行治疗功能的分子工具。
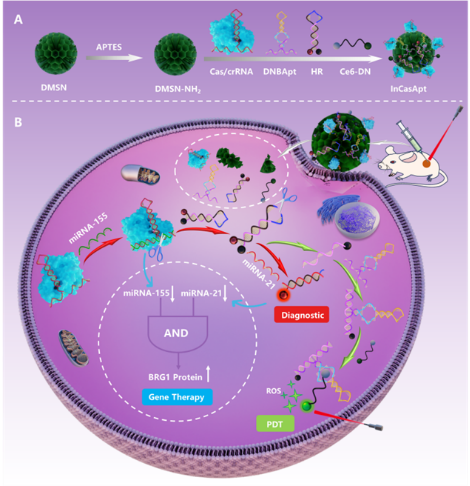
本研究开发了一种miRNA逻辑“与”门激活的RNA装置(InCasApt)用于精确诊断和治疗。InCasApt系统包括Cas13a/crRNA,发夹报告探针(HR),二硝基苯胺(DN)封装的Ce6(Ce6-DN),以及DN结合RNA适配体前体(DNBApt),这些组分共同负载在树状介孔硅纳米颗粒(DMSN)上。在正常细胞中,纳米InCasApt装置保持惰性。在肿瘤细胞中,升高的miRNA-155激活Cas13a的核酸酶活性来切割HR,miRNA-21随后取代HR中猝灭剂染料标记的换能器序列(TS),诱导荧光恢复用于实现诊断目的。释放的TS折叠并激活DNBApt,恢复结合的Ce6-DN的光敏能力,用于精确的光动力治疗(PDT)。此外,InCasApt系统实现了miRNA-155和miRNA-21功能的抑制,导致抗基因BRG1上调,抑制肿瘤迁移。因此,在体外和体内,InCasApt都可以通过内源性miRNA和逻辑门激活联合基因治疗和PDT抑制肿瘤细胞的生长。
本研究得到了国家自然科学基金、深圳市医学研究专项资金项目、广东省珠江团队项目和深圳市纳米生物传感技术重点实验室等资助。
原文链接:https://pubs.acs.org/doi/full/10.1021/jacs.4c08719
撰稿:杨琦琦 审核:陆敏华