在精准医疗与即时诊断技术快速发展的今天,血液检测被认为是实现疾病早筛与疗效动态监测的重要方向。然而,疾病早期的生物标志物(蛋白、DNA/RNA 等)往往浓度极低,传统检测常依赖核酸扩增或复杂前处理,存在耗时、成本高、流程繁琐等问题。
张晗教授团队依托深圳大学射频异质异构重点实验室在Optica发表题为“Sub-Attomolar-Level Biosensing of Cancer Biomarkers Using SHG Modulation in DNA-Programmable Quantum Dots/MoS2 Disordered Metasurfaces”的研究论文,深圳大学为第一完成单位和通讯作者单位,杜博文助理教授与田曦麟博士生为共同第一作者。通过融合二维材料非线性光学读出、DNA 纳米结构精确组装与 CRISPR 分子识别技术,他们尝试构建一种光学传感平台,以期在无需核酸扩增的情况下,实现对肺癌相关 miRNA 等生物标志物的超低浓度检测。这项研究或许能为疾病早期筛查提供一种高灵敏度、低背景噪声的参考思路。
无需扩增即可检测极低浓度标志物这一目标实现一直面临挑战。传统血液检测往往依赖核酸扩增或复杂的前处理流程,存在耗时、成本高且容易引入污染的问题。这次的论文提供了新解决方案尝试:利用二次谐波(SHG)作为信号读出机制。SHG 属于非线性光学过程,可将入射光转换为波长减半的输出信号,其天然具备背景噪声低的优势,使其适合捕捉“极少分子”带来的微弱变化。研究团队将量子点引入二硫化钼(MoS₂)表面附近,通过量子工程能量转移与局域场增强,试图提升非线性光学响应。有助于在复杂生物基质中获得更高的信噪比与更稳定的检测窗口。
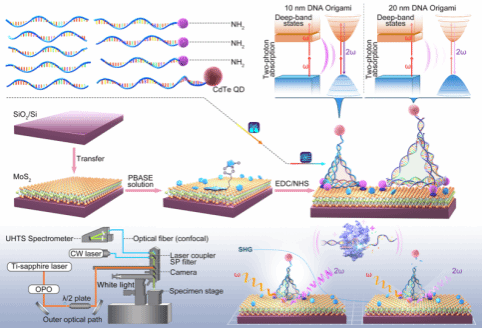
图1. 利用DNA正四面体构建的QD/MoS2无序超表面的设计
在研究中,团队设计了一种MoS₂/DNA 正四面体/QD结合 CRISPR-Cas12a 生物识别模块的核心结构。利用 DNA 纳米结构将量子点以纳米级精度定位到 MoS₂表面附近,从而增强 SHG 信号;当靶标分子存在时,CRISPR-Cas12a 被激活并切割用于固定量子点的 DNA 连接结构,导致量子点状态发生改变,进而引发 SHG 信号出现可测下降。这种设计旨在将分子识别事件直接转化为光学信号变化的读出,避免了传统方法中复杂的信号放大步骤该平台在测试浓度覆盖 10 fM 到 100 zM 的范围内均表现出一定的响应,并在 100 zM 的超低浓度下仍能获得可分辨的 SHG 信号变化。同时在保持高灵敏度的情况下,该体系具备单碱基分辨能力,这意味着它可能区分极其相似的基因序列。
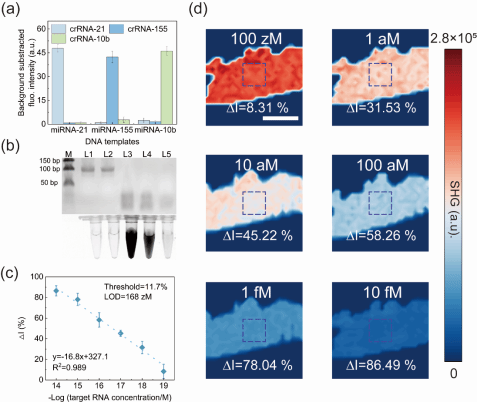
图2 量子点/MoS2无序超表面中的二次谐波生物传感
研究团队用协同设计框架来解释这一性能表现。SHG 读出的低背景噪声特性是关键,它试图解决弱光 - 物质相互作用带来的信号瓶颈。DNA 结构的可编程性与 CRISPR 靶向识别的灵活性相结合,有助于在复杂生物基质中获得更高的信噪比与更稳定的检测窗口。在 800 nm 飞秒激光激发下,系统记录了最终的 SHG 特征光谱。当然,本实验还有一些限制,虽然实现了无需扩增,但目前的光学系统仍依赖共聚焦显微镜,距离真正的便携化还有距离;其次,SHG 信号虽然背景低,但对实验环境稳定性要求较高,后续工程化需要解决抗干扰问题。该体系目前主要针对肺癌相关 miRNA,其他疾病标志物的适用性还需进一步探索。并且研究实际描述的是一种技术路径上的可行性,这种光学传感平台在特定条件下确实能实现超低浓度检测,这是一个条件性的优势,高度依赖设备小型化和成本控制。后续团队计划推进光学系统的小型化与便携化,尝试应用于床旁、门诊乃至低资源地区的快速检测场景。
论文信息
论文题目:Sub-attomolar-level biosensing of cancer biomarkers using SHG modulation in DNA-programmable quantum dots/MoS₂ disordered metasurfaces
DOI:10.1364/OPTICA.577416